Dimetyyliheptyylipyraani
| Dimetyyliheptyylipyraani | |
|---|---|
 |
|
| Tunnisteet | |
| IUPAC-nimi | 6,6,9-trimetyyli-3-(3-metyyli-2-oktanyyli)-7,8,9,10-tetrahydro-6H-bentso[c]kromen-1-oli |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | C25H38O2 |
| Moolimassa | 370,57 g/mol |
| Liukoisuus veteen | Liukenee alkoholiin ja poolittomiin liuottimiin, ei liukene veteen. |
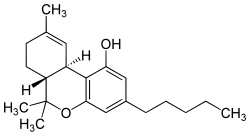
Dimetyyliheptyylipyraani (DMHP) on äärimmäisen voimakas synteettinen THC-johdannainen kemikaali.
Kemikaali keksittiin vuonna 1949 tutkittaessa Δ9-THC:n - joka on yksi kannabiksen vaikuttavista aineista - rakennetta.[1] DMHP on kellertävää, viskoottista ja öljymäistä nestettä; joka ei liukene veteen, mutta liukenee alkoholiin ja poolittomiin liuottimiin.
DMHP on rakenteellisesti samankaltainen THC:n kanssa, poiketen ainoastaan että molekyylissä on yksi kaksoissidos eri kohdassa, ja siinä 3-fenyyliketju on korvautunut 3-(1,2-dimetyylifenyyli)-ketjulla.[2] Kemikaali on vaikutuksiltaan THC:n kaltainen, mutta huomattavasti voimakkaampi[3], erityisesti kipua lievittäviltä ja kouristuksia ehkäiseviltä vaikutuksiltaan. Sillä on kuitenkin verrattaen miedompi psyykkinen vaikutus. DMHP:n on arveltu olevan CB1-reseptorin agonisti, muiden kannabinoidijohdannaisten tavoin.[4]
DMHP:n käyttöä mahdollisena ei-kuollettavana kemiallisena aseena on tutkittu Yhdysvalloissa[5], sen voimakkaasti keskushermostoa lamaavan vaikutuksensa vuoksi.
Kemikaalin eliminaation puoliintumisaika on 20–39 tuntia, ja sen aktiivisen metaboliitin 11-hydroksi-DMHP:n puoliintumisaika puolestaan on yli 48 tuntia.
DMHP:lla on seitsemän kaksoissidosisomeeria, ja niillä yhteensä 120 stereoisomeeria.
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ Adams R, Harfenist M, Loewe S (1949). "New Analogs of Tetrahydrocannabinol. XIX". Journal of the American Chemical Society 71 (5): 1624. doi:.
- ↑ Razdan RK (1980). "The Total Synthesis of Cannabinoids", Total Synthesis of Natural Products, Volume 4. Wiley-Interscience. DOI:10.1002/9780470129678.ch2. ISBN 9780471054603.
- ↑ "Slowing of cortical somatosensory evoked activity by delta 9-tetrahydrocannabinol and dimethylheptylpyran in alpha-chloralose-anesthetized cats" (1982). Neuropharmacology 21 (7): 705–9. doi:. PMID 6289158.
- ↑ "Cannabinoid agonists and antagonists modulate lithium-induced conditioned gaping in rats" (2003). Integrative physiological and behavioral science : the official journal of the Pavlovian Society 38 (2): 133–45. doi:. PMID 14527182.
- ↑ (1984) Possible Long-Term Health Effects of Short-Term Exposure To Chemical Agents Vol. 2: Cholinesterase Reactivators, Psychochemicals and Irritants and Vesicants. Commission on Life Sciences. The National Academies Press, 79–99.
